Ниже прилагаю Mapping Document — сравнение текущей и предлагаемой структуры регистрационного досье.
Руководство ICH M4Q(R2), регулирующее структуру CTD, еще не принято (проект приложила ниже), но уже сейчас можно посмотреть, что нового.
Информация будет организована по компонентам лекарственного препарата, а именно:
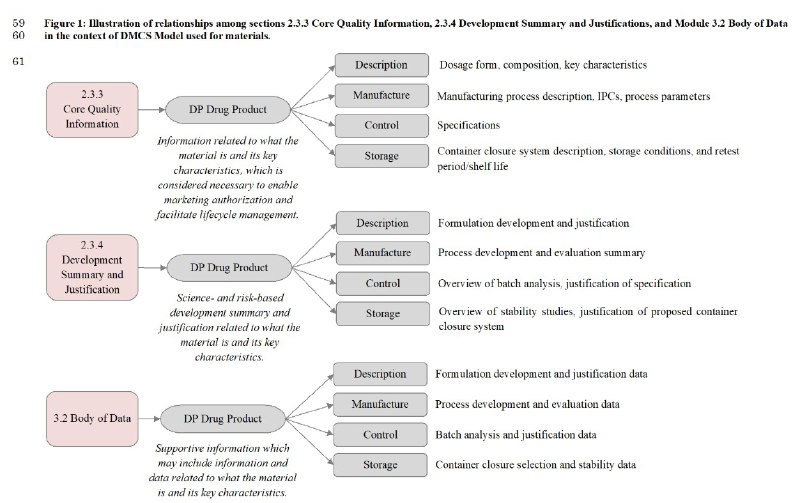
Drug Substances (DS), Substance Intermediates (SI), Raw Materials (RM), Starting Materials (SM), Reference Standards/Materials (RS), Excipients (EX), Impurities (IM), Drug Products (DP), Product Intermediates (PI), Packaged Medicinal Products (PM), Pharmaceutical Products (PH), and Medical Devices (MD).Изложение будет следовать модели DMCS, расшифровывающейся как Description, Manufacture, Control, and Storage. Пример для лекарственного препарата Drug Product (DP) на картинке к посту я позаимствовала как раз из проекта руководства.
С Новым годом (я до Китайского Нового года буду вас поздравлять), с новым регдосье!
✍️ Ваш Переводчик без...

Дискуссия